Н.П. ЛУКУТЦОВА, канд. техн. наук,
Брянская государственная инженерно-технологическая академия
Тяжелые металлы (медь, цинк, никель, свинец, хром, кобальт, кадмий) попадают в строительные материалы с природным и техногенным сырьем.
В породах естественного происхождения всегда присутствуют кроме основных и второстепенных компонентов тяжелые металлы. Наименьшее их количество содержится в карбонатных, наибольшее — в глинистых породах. Промышленные отходы более обогащены тяжелыми металлами. Превышение предельно допустимых концентраций (ПДК) наблюдается в пиритных огарках, золе, фосфогипсе, минеральных шламах, отработанных формовочных смесях (ОФС) и др.
По валовому содержанию тяжелых металлов в некоторых промышленых отходах предприятий Брянской области превышение ПДК составляет: по свинцу от 1,3 до 45 раз, по меди от 1,2 до 225 раз, по цинку от 1,4 до 21 раза и по никелю в 5,7 раза.
При использовании техногенного сырья в производстве строительных материалов в соответствии с МУ 2.1.674—97. «Санитарно-гигиеническая оценка стройматериалов с добавлением промотходов» [1] необходимо, чтобы содержание водорастворимых форм тяжелых металлов не превышало предельно допустимых концентраций для вод поверхностных водоемов (ПДКв) [2], так как воздействие агрессивных сред, механические повреждения и другие факторы могут привести к нарушению целостности изделия, его конструкции и способствовать миграции из строительного материала опасных компонентов. Поэтому необходимо обеспечить надежное связывание тяжелых металлов в структурно устойчивые соединения, чтобы не происходила их эмиссия и вторичное загрязнение окружающей среды.
С целью выявления механизмов миграции и связывания тяжелых металлов образцы из цементного бетона с заполнителем из ОФС (отходы Брянского сталелитейного завода) состава Ц:ОФС = 1:3 при водоцементном отношении В/Ц = 0,5 выдерживались в агрессивных средах в течение 10—30 сут.
Как показали исследования, с течением времени происходит увеличение концентрации тяжелых металлов в окружающей образец среде (табл. 1). Так, через месяц экспозиции песчаного бетона на ОФС во всех исследуемых средах наблюдается превышение ПДКв по свинцу двухвалентному (Pb2+) и шестивалентному хрому (Cr6+) до 20 и 43 раз соответственно. Для меди, цинка, кобальта и никеля концентрация в агрессивных средах, за исключением никеля в 2% серной кислоте, значительно ниже ПДКв. При этом значения рН среды во времени претерпевают существенные изменения. Для щелочных и нейтрально-водных сред значения рН выше 7 можно объяснить либо вымыванием основных оксидов (СаО и др.) из бетона, либо собственной высокой щелочностью (растворы КОН, NaOH, Na2CO3 и т. д.). В случае применения в качестве агрессивных сред растворов НС1 и H2SO4 рост значения рН до 11,6—13,45 связан вероятнее всего с процессом коррозии. В кислых агрессивных средах при первоначально низких значениях рН (менее 3) происходит нейтрализация кислоты в результате взаимодействия с основными оксидами (СаО и MgО) вплоть до полного ее расхода. При этом увеличивается пористость, способствующая дальнейшему эффективному вымыванию СаО и других щелочных агентов наряду с катионами тяжелых металлов в виде растворимых солей, за исключением свинца (PbSO4 и PbCl2 плохо растворимы в воде). В результате со временем значения рН среды вытяжек из кислых переходят в сильнощелочные.
Таблица 1
|
Среда |
Концентрация металлов в вытяжках через 30 сут экспозиции образцов бетона на ОФС , мг/л |
||||||||
|
рН исходное |
рН вытяжки |
Pb2+ |
Cu |
Fe |
Ni |
Co |
Zn |
Cr6+ |
|
| 2,5% Na2CO3 |
8,2 |
12,2 |
0,15 |
0,005 |
0,09 |
<0,006 |
0,028 |
0,004 |
1 |
| 2,5% CaCO3 |
10,75 |
10,25 |
0,083 |
0,013 |
0,077 |
<0,006 |
<0,006 |
0,031 |
0,321 |
| Дистиллированная вода |
6,5 |
9,9 |
0,05 |
0,003 |
0,07 |
<0,006 |
<0,006 |
0,009 |
0,64 |
| Водопроводная вода |
7,85 |
10,35 |
0,06 |
0,019 |
0,09 |
0,007 |
<0,006 |
0,01 |
0,93 |
| 0,1 н. HCl |
— |
11,6 |
0,086 |
0,01 |
0,093 |
0,013 |
0,043 |
0,009 |
0,07 |
| 2% H2SO4 |
2,5 |
13,45 |
0,054 |
0,205 |
11,64 |
0,157 |
0,088 |
0,559 |
0,146 |
| 2,5% KOH |
13,7 |
13,7 |
0,853 |
0,029 |
0,903 |
<0,006 |
<0,006 |
0,527 |
0,361 |
| 2,5% NaOH |
12,65 |
12,65 |
1,24 |
0,027 |
0,248 |
0,014 |
<0,006 |
0,431 |
0,177 |
| 2,5% MgCl2 |
6,35 |
8,4 |
0,168 |
0,021 |
0,015 |
0,012 |
<0,006 |
0,024 |
0,058 |
| 2,5% MgSO4 |
6 |
8,95 |
0,108 |
0,003 |
0,019 |
<0,006 |
<0,006 |
0,011 |
0,113 |
| 2,5% Na2S04 |
6,2 |
12,5 |
0,17 |
0,003 |
0,1 |
0,012 |
0,007 |
0,008 |
0,61 |
| 2,5/% K2SO4 |
5,8 |
12,5 |
0,15 |
0,005 |
0,06 |
0,013 |
0,01 |
0,005 |
0,39 |
| ПДК для вод поверхностных водоемов |
— |
0,03 |
1 |
— |
0,1 |
0,1 |
1 |
0,05 |
|
| Превышение ПДК |
— |
1,6-43 |
нет |
3-38,8 |
нет |
нет |
нет |
1,16-20 |
|
Установлено, что степень вымывания катионов в щелочных средах резко возрастает в тех случаях, когда оксид металла обладает амфотерным свойством. Если в дистиллированной воде и щелочных средах медь вымывается примерно в одинаковых количествах, то металлы амфотерных оксидов (железо, никель, кобальт, цинк и свинец) проявляют тенденцию усиления миграции с повышением рН среды. Количество вымываемого оксида амфотерного металла зависит от его содержания в бетоне, растворимости в воде его гидроксида и от рН начала растворения. Гидроксид цинка начинает растворяться при рН выше 10,5 [3]. Поэтому в сильнощелочных средах содержание цинка в вытяжках соизмеримо с содержанием железа, хотя его начальная концентрация намного ниже, чем железа.
Свинец в бетоне находится в подвижных водорастворимых соединениях. Растворяясь в щелочах, Pb(OH)2 образует плюмбиты Са[Pb(OH)4] и гидроксо-плюмбиты Са2[ Рb(ОН)6].
Характер кривой изменения концентрации свинца в водных средах образцов песчаного бетона на ОФС (1:3, В/Ц = 0,5) естественного твердения от времени экспозиции свидетельствует, что процесс вымывания Pb2+ на протяжении всего периода экспозиции (30 сут) контролируется диффузией (рис.).
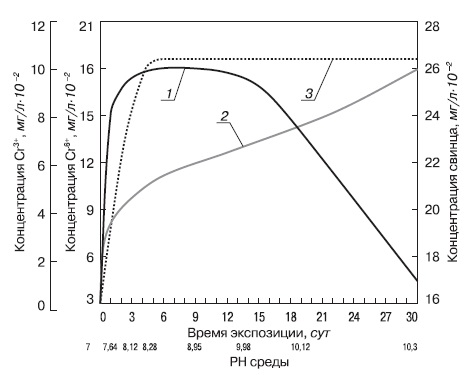
Зависимость концентрации хрома и свинца в водных вытяжках образцов песчаного бетона на ОФС (1:3, В/Ц=0,5) естественного твердения от времени экспозиции и рН среды: 1 — Cr3+; 2 — Cr6+; 3 — Pb2+
Динамика накопления Cr3+ и Cr6+ катионов в воде указывает, что они появляются в вытяжках одновременно. С течением времени при повышении рН среды содержание Cr3+ в воде не меняется вплоть до 12 сут выдержки. В дальнейшем с ростом рН содержание Cr3+ резко уменьшается (примерно в 10 раз). Это сопровождается увеличением содержания Cr6+ до 26-10-2 мг/л. Гидроксид хрома Сг(ОН)3 начинает растворяться при значениях рН больше 12 [3]. Следовательно, уменьшение содержания Cr3+ начиная с рН = 10 не может быть объяснено растворением его амфотерных соединений. С учетом постоянства суммы двух форм хрома в растворе уменьшение содержания Cr3+ объясняется протеканием окислительно-восстановительной реакции, при которой Cr3+ окисляется в Cr6+.
В качестве окислителя выступают катионы Fe3+, содержание которых в водных вытяжках намного превышает суммарное содержание всех других катионов.
В щелочных средах Cr6+ образует водорастворимые хроматы, в связи с чем наблюдаются аномально высокие значения количества вымываемого хрома при его невысоком начальном содержании в бетоне. Соединения Cr6+ в зависимости от рН среды в водных растворах находятся в виде различных форм — бихроматов или хроматов.
Окислительно-восстановительную реакцию между Cr3+ и Fe3+ в щелочной среде можно представить в виде полуреакций (а, б):
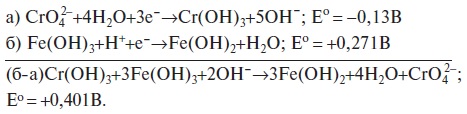
Электродный потенциал полуреакции (б) выше, чем полуреакции (а), из чего следует, что процесс (б) будет иметь место в прямом, а процесс (а) — в обратном направлении.
Учитывая, что медь, цинк, никель, кобальт надежно блокируются в составе бетона, а водой вымываются свинец и шестивалентный хром, для связывания последних в бетоне исследовались различные виды добавок.
При этом необходимо было учесть следующее. Во-первых, добавки должны обеспечивать концентрации свинца и хрома в водных вытяжках ниже ПДКв. Во-вторых, они не должны ухудшать свойств бетонов, а по возможности их улучшать. В-третьих, при связывании одновременно свинца и шестивалентного хрома добавки должны быть совместимые. В-четвертых, они должны быть доступными и дешевыми.
Наиболее эффективными добавками для снижения концентрации шестивалентного хрома в водных вытяжках из бетона оказались щавелевая кислота и хлористый барий, а для свинца — карбонат кальция и дитизон. Концентрация Cr6+ и Pb2+ в водных вытяжках из песчаного бетона на ОФС через 10 сут экспозиции при использовании комплексных добавок приведена в табл. 2.
Таблица 2
|
Добавки, мас. % от количества ОФС в бетоне |
Концентрация тяжелых металлов в водных вытяжках, мг/л |
|
|
Сг6+ |
Pb2+ |
|
| BaCl2 0,01%+CaCO3 0,3% |
<0,006 |
0,0235 |
| Н2С2О4-2Н20 0,01%+CaCO3 0,3% |
<0,006 |
0,0188 |
| BaCl2 0,01%+KI 0,03% |
<0,006 |
0,0324 |
| Н2С2О4-2Н20 0,01%+KI 0,03% |
<0,006 |
0,0311 |
| BaCl2 0,01%+дитизон 0,01% |
<0,006 |
0,0162 |
| Н2С2О4-2Н20 0,01%+дитизон 0,01% |
<0,006 |
0,0183 |
| BaCl2 0,01%+СаСО3 0,5% |
<0,006 |
<0,006 |
| Н2С2О4-2Н20 0,01%+дитизон 0,02% |
<0,006 |
<0,006 |
| ПДКв, мг/л |
0,05 |
0,03 |
| Примечание. Песчаный бетон состава 1:3, В/Ц=0,45. | ||
Установлено, что при введении в бетоны на ОФС щавелевой кислоты (0,01 мас. % от массы ОФС в бетоне) и хлорида бария (0,01%) в водных вытяжках не были обнаружены соединения шестивалентного хрома. Содержание свинца снижается до <0,006 мг/л при введении добавок карбоната кальция (0,5%) и дитизона (0,02%). При совместном использовании добавок хлорида бария (0,01%) и карбоната кальция(0,5%) или щавелевой кислоты (0,01%) и дитизона (0,02%) концентрация Cr6+ и Pb2+ в водных вытяжках составляет менее 0. 006.мг/л.
Выявлены особенности процесса структурообразования песчаного бетона, содержащего ОФС в присутствии тяжелых металлов и комплексных добавок, которые позволили не только связать свинец и хром в малорастворимые устойчивые к вымыванию соединения, но и повысить на 15—40% предел прочности при сжатии в ранние сроки твердения (табл. 3).
Таблица 3
|
Вид и количество добавки |
Предел прочности при изгибе, МПа |
Предел прочности при сжатии, МПа |
|||
|
Время твердения, сут |
Пропаривание |
||||
|
7 |
14 |
28 |
|||
| Без добавки |
3 |
6,1 |
7,5 |
14,2 |
15,6 |
| ВаС12 0,03%+СаСО3 0,5% |
1,9 |
7,7 |
8,8 |
14,7 |
16,4 |
| ВаС12 0,03%+дитизон 0,01% |
2 |
7,3 |
9,9 |
14,8 |
16,4 |
| H2C2O4-2H2O 0,01%+СаСО3 0,5% |
1,9 |
7,8 |
8,1 |
13,9 |
14,8 |
| H2C2O4-2H2O 0,01%+дитизон 0,01% |
2,1
|
8,6
|
10,3
|
14,4
|
16,6
|
| Примечание. Бетон состава 1:3, В/Ц=0,44. | |||||
Таким образом, установлено, что механизм и динамика накопления катионов тяжелых металлов, таких как Cr3+ и Cr6+, Pb2+, цинк, медь, никель, кобальт, в водных вытяжках из песчаных бетонов, содержащих отработанные формовочные смеси, связаны с сочетанием одновременно протекающих диффузионных и химических процессов кислотно-основного взаимодействия.
Медь, цинк, никель, кобальт блокируются в составе бетона в отличие от катионов свинца и хрома.
Наиболее эффективным способом снижения концентрации свинца и хрома является химическое связывание катионов в устойчивые малорастворимые соединения добавками щавелевой кислоты (0,01%), хлористого бария (0,01%), карбоната кальция (0,5%), дитизона (0,01%), а также комплексными добавками на их основе.
Список литературы
- МУ 2.1.674—97. Санитарно-гигиеническая оценка стройматериалов с добавлением промотходов. М.: Минздрав России. 1997. 40 с.
- СанПиН 4630—88. Санитарные правила и нормы охраны поверхности вод от загрязнения / Минздрав СССР. Главное санэпидуправление. М., 1988. 70 с.
- Лурье Ю.Ю. Справочник по аналитической химии. М.: Химия. 1971.454 с. (с. 248).
Статья взята из журнала «Строительные материалы»